年龄相关性白内障(age-related cataract)是最常见的白内障类型。通过裂隙灯进行检查,60岁以上老年人中大约96%可以发现晶状体有不同程度或不同形式的混浊。不过大多数病例病情进展缓慢,且不影响视力。在部分病例确实因晶状体混浊而影响视力,此时年龄相关性白内障的诊断才真正具有临床意义。 年龄相关性白内障是指中老年开始发生的晶状体混浊,随着年龄增加,患病率明显增高。由于它主要发生于老年人,以往习惯称之为老年性白内障。它的发生与环境、营养、代谢和遗传等多种因素有关。一般认为,氧化损伤在这类白内障的形成过程中起主要作用。流行病学研究表明,紫外线照射、酗酒、吸烟、妇女生育多、心血...[详细]
不同类型的白内障,其致病危险因素及发病机制亦不同。详细的病因学研究可以区别不同危险因素在白内障形成过程中的作用,仍然是一个复杂而困难的课题。以某种危险因素作为某种类型白内障形成原因,建立不同类型白内障动物模型,对于总结众多危险因素在白内障病因学中的作用是一种非常有价值的研究方法。虽然这种模型有一定的局限性,比如它往往忽略了白内障形成过程中时间的影响和不同的危险因素致白内障的复杂性,但在揭示白内障形成和发生发展过程中的规律性的作用却不容怀疑。 白内障的发生是多种因素综合作用的结果,比如放射和自由基损伤;营养物质、化学物质缺乏和抗生素的使用;葡萄糖、半乳糖等代谢障碍;脂质过氧化产物损伤...[详细]
1.抗氧化系统 氧自由基损伤是老年性白内障首位的危险因素。许多实验都证明晶状体的氧化损伤发生在晶状体混浊之前。各种理化因素均可通过不同途径导致晶状体自由基产生,如自由基产生过多或清除障碍,均可导致自由基聚积。自由基最先损害的靶目标是晶状体上皮细胞,其次是晶状体纤维。致使蛋白质和脂质过氧化,发生交联、变性,并聚积成大分子。 晶状体上皮细胞是抗氧化损伤的活性中心,通过两个途径发挥抗氧化作用。第一个途径是以还原型谷胱甘肽(GSH)、维生素C和维生素E等抗氧化剂为代表的清除自由基机制。晶状体的氧化损伤最早表现在GSH含量大幅度下降,氧化型谷胱甘肽(GSSG)增加,GSH/GSSG比值降低。...[详细]
根据混浊部位的不同,临床上将年龄相关性白内障分为3种类型,即皮质性、核性和后囊膜下混浊性白内障。事实上,各类型年龄相关性白内障之间无严格区分,仅仅是代表混浊以何部位为主导的情况。皮质性在年龄相关性白内障最为常见,占65%~70%;其次为核性白内障,占25%~35%;囊膜下混浊性白内障相对比较少见,仅占5%。 1.皮质性年龄相关性白内障 皮质性白内障(cortical cataract)是年龄相关性白内障中最常见的一种类型,其特点是混浊自周边部浅皮质开始,逐渐向中心部扩展,占据大部分皮质区。根据其临床发展过程及表现形式,皮质性白内障可分为4期:初发期、进展期、成熟期和过熟期。...[详细]
在年龄相关性白内障发展的不同时期可能出现闭角型青光眼的急性发作,晶状体成分过敏性眼内炎、晶状体溶解性青光眼以及晶状体核脱入玻璃体等。
开展的多是与白内障手术相关的一些必要的全身检查,如血常规,血液生化检查、尿常规等检查。了解病人身体的基本状态,并可以排除白内障发病的其他危险因素。
可以预测手术中出现的异常情况以及术后视力。 1.眼压检查 排除高眼压引起的视功能损害。 2.房角检查 应用房角镜、超声生物显微镜(ultrasound biomicroscopy,UBM)进行房角的检查,以了解虹膜角膜角的宽窄和开放程度,主要是在伴有青光眼史的患者中,为手术方式的制定提供依据。 超声生物显微镜检查是目前了解眼前段组织结构的一种重要方法,它能够检查虹膜、房角、晶状体及其悬韧带情况,特别是在眼前段屈光间质混浊或小瞳孔时,是白内障手术前一种重要的辅助诊断手段(图 6)。 3.B超检查(B-ultrasonic Scanning) 对...[详细]
根据病史、临床表现及临床检查体征可以明确诊断。在有关白内障的流行病学调查中,由于诊断标准不同,研究结果将有很大差异。各研究资料之间难于进行相互比较,因此必须制定出明确的诊断标准和规范的调查方法。目前,我国采用的白内障流行病学调查,主要参照如下3个标准来进行。 1.世界卫生组织(WHO)盲与低视力标准 矫正视力<0.05为盲;≥0.05~<0.3为低视力; 2.WH0与美国国家眼科研究所诊断标准 1982年WHO与美国国家眼科研究所提出,视力<0.7、晶状体混浊,而无其他导致视力下降的眼病作为白内障诊断标准。 3.特定年龄段标准 专为调查某一年龄段的白内...[详细]
1.药物治疗 包括含硫制、抗醌体制剂、醛糖还原酶抑制剂、维生素及能量合剂、天然提取物等,如法可利晴、谷胱甘肽、维生素C、仙诺林特、白内停等。可以进行局部或全身治疗。 2.手术治疗 是治疗白内障的最基本、最有效的方法。目前主要采用白内障超声乳化联合人工晶体植入技术。
与眼球本身状态及眼底病变情况密切相关。
避免紫外线照射,服用抗氧化及抗自由基药物等对于部分病人有效。


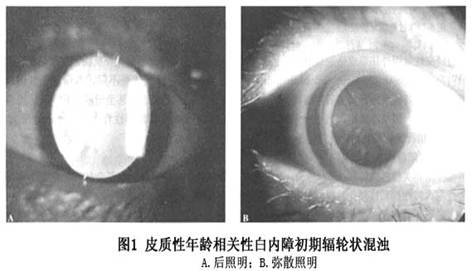 (2)进展期:晶状体纤维水肿和纤维间液体的不断增加,使晶状体发生膨胀,厚度增加,因此也被称作膨胀期。一方面因以混浊为背景的囊膜张力增加而呈现绢丝样反光;另一方面,由于膨胀的结果而使前房变浅。后者在一个有青光眼体质的患者,很容易诱发青光眼的急性发作。但并非所有皮质性白内障患者都要经历膨胀期发展过程。即使有,其持续时间及严重程度个体间存在相当大的差异,不一定都会诱发青光眼发作。这一阶段患者主要症状为视力逐渐减退,有时伴有眩光感,偶有单眼复视者。由于尚有一部分皮质是透明的,因此虹膜新月影投照试验是阳性(图2)。
(2)进展期:晶状体纤维水肿和纤维间液体的不断增加,使晶状体发生膨胀,厚度增加,因此也被称作膨胀期。一方面因以混浊为背景的囊膜张力增加而呈现绢丝样反光;另一方面,由于膨胀的结果而使前房变浅。后者在一个有青光眼体质的患者,很容易诱发青光眼的急性发作。但并非所有皮质性白内障患者都要经历膨胀期发展过程。即使有,其持续时间及严重程度个体间存在相当大的差异,不一定都会诱发青光眼发作。这一阶段患者主要症状为视力逐渐减退,有时伴有眩光感,偶有单眼复视者。由于尚有一部分皮质是透明的,因此虹膜新月影投照试验是阳性(图2)。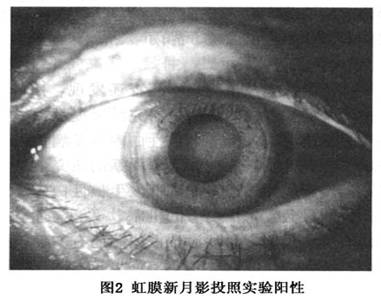 (3)成熟期:这一阶段以晶状体全部混浊为其特点。裂隙灯检查仅能看到前面有限深度的皮质,呈无结构的白色混浊状态。此时虹膜新月影投照试验转为阴性。晶状体纤维经历了水肿、变性、膜破裂等一系列病理过程,最终以晶状体纤维崩溃,失去正常形态为结局。组织学上,代表纤维基质变性的特征性改变,形成所谓Morgagnian小体。应用组织化学技术及X线衍射方法,对糖尿病和年龄相关性白内障晶状体进行研究发现,球样小体具有脂质双层膜,其内含有γ-晶状体蛋白、少量α-和β-晶状体蛋白及肌纤维蛋白,证明其纤维基质来源。 至成熟期阶段,晶状体囊膜尚能保持原有的韧性和张力,此后逐渐向变性发展。因此在白内障成熟之前行囊外白内障摘除、超声乳化白内障吸除及人工晶状体植入术是恰当的。 (4)过熟期:由于基质大部分液化,某种基本成分的丧失,使晶状体内容减少,前囊膜失去原有的张力而呈现松弛状态(图3)。有时可看到尚未液化的核心沉到囊袋下方,随眼球转动而晃动。此时,可伴有虹膜震颤。在特殊情况下,因外伤或剧烈震动可使核心穿破囊膜而脱入前房或玻璃体腔。如伴有液化基质流失,患者会出现豁然开朗的不治而愈的结果。
(3)成熟期:这一阶段以晶状体全部混浊为其特点。裂隙灯检查仅能看到前面有限深度的皮质,呈无结构的白色混浊状态。此时虹膜新月影投照试验转为阴性。晶状体纤维经历了水肿、变性、膜破裂等一系列病理过程,最终以晶状体纤维崩溃,失去正常形态为结局。组织学上,代表纤维基质变性的特征性改变,形成所谓Morgagnian小体。应用组织化学技术及X线衍射方法,对糖尿病和年龄相关性白内障晶状体进行研究发现,球样小体具有脂质双层膜,其内含有γ-晶状体蛋白、少量α-和β-晶状体蛋白及肌纤维蛋白,证明其纤维基质来源。 至成熟期阶段,晶状体囊膜尚能保持原有的韧性和张力,此后逐渐向变性发展。因此在白内障成熟之前行囊外白内障摘除、超声乳化白内障吸除及人工晶状体植入术是恰当的。 (4)过熟期:由于基质大部分液化,某种基本成分的丧失,使晶状体内容减少,前囊膜失去原有的张力而呈现松弛状态(图3)。有时可看到尚未液化的核心沉到囊袋下方,随眼球转动而晃动。此时,可伴有虹膜震颤。在特殊情况下,因外伤或剧烈震动可使核心穿破囊膜而脱入前房或玻璃体腔。如伴有液化基质流失,患者会出现豁然开朗的不治而愈的结果。 当囊膜变性或因外伤形成微细裂痕时,蛋白成分可溢入前房,诱发自身免疫反应,引起晶状体成分过敏性眼内炎(phaco-anaphylactic endophthalmitis)。与一般性虹膜睫状体炎不同,本病发病急骤,突然出现眼睑肿胀、角膜水肿,角膜后羊脂样KP分布密集,广泛虹膜后粘连,甚至形成瞳孔膜闭。而组织碎片可积聚于虹膜角膜角,阻塞小梁网,从而产生继发性青光眼,即所谓晶状体溶解性青光眼(phacolytic glaucoma)。大多数情况下,药物治疗无效,手术摘除晶状体是惟一的手段。 2.核性年龄相关性白内障 核性年龄相关性白内障(nuclear cataract)远不像皮质性白内障那样具有复杂的形态学变化和发展阶段。核性白内障往往和核硬化并存。最初,混浊出现在胚胎核,尔后向外扩展直到老年核。这一过程可持续数月、数年或更长的时间。在晶状体核混浊过程中可伴随着颜色的变化。早期,少量棕色色素仅仅积聚在核区而不向皮质区扩展。但有时皮质区很薄,也可呈现整个晶状体均呈棕色反光的外观。当色素积聚较少时,核心部呈淡黄色,对视力可不造成影响,眼底亦清晰可见,裂隙灯检查可在光学切面上以密度差别勾画出混浊的轮廓(图4)。
当囊膜变性或因外伤形成微细裂痕时,蛋白成分可溢入前房,诱发自身免疫反应,引起晶状体成分过敏性眼内炎(phaco-anaphylactic endophthalmitis)。与一般性虹膜睫状体炎不同,本病发病急骤,突然出现眼睑肿胀、角膜水肿,角膜后羊脂样KP分布密集,广泛虹膜后粘连,甚至形成瞳孔膜闭。而组织碎片可积聚于虹膜角膜角,阻塞小梁网,从而产生继发性青光眼,即所谓晶状体溶解性青光眼(phacolytic glaucoma)。大多数情况下,药物治疗无效,手术摘除晶状体是惟一的手段。 2.核性年龄相关性白内障 核性年龄相关性白内障(nuclear cataract)远不像皮质性白内障那样具有复杂的形态学变化和发展阶段。核性白内障往往和核硬化并存。最初,混浊出现在胚胎核,尔后向外扩展直到老年核。这一过程可持续数月、数年或更长的时间。在晶状体核混浊过程中可伴随着颜色的变化。早期,少量棕色色素仅仅积聚在核区而不向皮质区扩展。但有时皮质区很薄,也可呈现整个晶状体均呈棕色反光的外观。当色素积聚较少时,核心部呈淡黄色,对视力可不造成影响,眼底亦清晰可见,裂隙灯检查可在光学切面上以密度差别勾画出混浊的轮廓(图4)。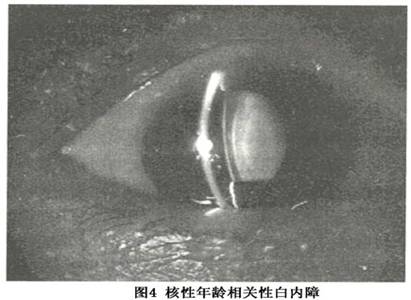 随着白内障程度加重,晶状体核颜色亦逐渐加深,由淡黄色转而变为棕褐色或琥珀色。在长期得不到治疗的所谓迁延性核性白内障病例,特别是糖尿病患者,晶状体核最终变为黑色,形成所谓的黑色白内障。晶状体核颜色与核硬度有一定的相关性,即颜色越深,核越硬,在拟行超声乳化手术前进行病例选择时尤应注意。从手术角度出发,鉴别皮质性和核性白内障的意义在于,前者的晶状体核一般较小并且比较软,最适合于超声乳化白内障吸除术;而后者在选择病例时,特别要考虑核硬度因素,这一点对初学者来说尤其重要。 值得提出的是,随着晶状体核硬化,屈光指数逐渐增加,从而形成了近视进行性增加的特殊临床现象。如果核硬化仅仅局限于胚胎核,而成年核不受影响,其结果将会产生一种更为特殊的双屈光现象,即中心区为高度近视,而外周区为远视,结果产生单眼复视。 3.囊膜下混浊性白内障 囊膜下混浊性白内障(subcapsular cataract)是指以囊膜下浅皮质混浊为主要特点的白内障类型(图5)。混浊多位于后囊膜下,呈棕色微细颗粒状或浅杯形囊泡状。有时前囊膜下也可出现类似改变。病变一般从后囊膜下视轴区开始,呈小片状混浊,与后囊膜无明显界限。在裂隙灯下检查时,有时可以发现混浊区附近的囊膜受累,呈现黄、蓝、绿等反射,形成所谓的多彩样闪辉(polychromatic luster)现象。由于病变距节点更近,因此即使病程早期,或病变范围很小很轻,也会引起严重的视力障碍。临床上,常常发现视力同晶状体混浊程度不相符合的情况,仔细检查方可发现后囊膜混浊是其主要原因。当前囊膜下出现类似改变时,囊膜下透明区消失,可演变成前囊膜下白内障。这种类型的白内障多发生在60~80岁年龄组。但在成熟期或过熟白内障,以晶状体全面陷入混浊为特点,其前囊膜下受累必然是一种并发现象,不应与此相混淆。
随着白内障程度加重,晶状体核颜色亦逐渐加深,由淡黄色转而变为棕褐色或琥珀色。在长期得不到治疗的所谓迁延性核性白内障病例,特别是糖尿病患者,晶状体核最终变为黑色,形成所谓的黑色白内障。晶状体核颜色与核硬度有一定的相关性,即颜色越深,核越硬,在拟行超声乳化手术前进行病例选择时尤应注意。从手术角度出发,鉴别皮质性和核性白内障的意义在于,前者的晶状体核一般较小并且比较软,最适合于超声乳化白内障吸除术;而后者在选择病例时,特别要考虑核硬度因素,这一点对初学者来说尤其重要。 值得提出的是,随着晶状体核硬化,屈光指数逐渐增加,从而形成了近视进行性增加的特殊临床现象。如果核硬化仅仅局限于胚胎核,而成年核不受影响,其结果将会产生一种更为特殊的双屈光现象,即中心区为高度近视,而外周区为远视,结果产生单眼复视。 3.囊膜下混浊性白内障 囊膜下混浊性白内障(subcapsular cataract)是指以囊膜下浅皮质混浊为主要特点的白内障类型(图5)。混浊多位于后囊膜下,呈棕色微细颗粒状或浅杯形囊泡状。有时前囊膜下也可出现类似改变。病变一般从后囊膜下视轴区开始,呈小片状混浊,与后囊膜无明显界限。在裂隙灯下检查时,有时可以发现混浊区附近的囊膜受累,呈现黄、蓝、绿等反射,形成所谓的多彩样闪辉(polychromatic luster)现象。由于病变距节点更近,因此即使病程早期,或病变范围很小很轻,也会引起严重的视力障碍。临床上,常常发现视力同晶状体混浊程度不相符合的情况,仔细检查方可发现后囊膜混浊是其主要原因。当前囊膜下出现类似改变时,囊膜下透明区消失,可演变成前囊膜下白内障。这种类型的白内障多发生在60~80岁年龄组。但在成熟期或过熟白内障,以晶状体全面陷入混浊为特点,其前囊膜下受累必然是一种并发现象,不应与此相混淆。 囊膜下混浊性白内障,除后囊膜下浅皮质受累外,其他部分的皮质和晶状体核均透明,因此属于软核性白内障类型。从这一点出发,囊膜下混浊性白内障是超声乳化手术的最好适应证。
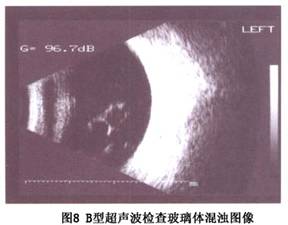
囊膜下混浊性白内障,除后囊膜下浅皮质受累外,其他部分的皮质和晶状体核均透明,因此属于软核性白内障类型。从这一点出发,囊膜下混浊性白内障是超声乳化手术的最好适应证。 3.B超检查(B-ultrasonic Scanning) 对于白内障患者是一种常规检查方法,可排除玻璃体积血、视网膜脱离和眼内肿瘤等疾患。在晶状体明显混浊,眼底镜检查不能辨明眼底情况时尤为重要(图7,8,9)。
3.B超检查(B-ultrasonic Scanning) 对于白内障患者是一种常规检查方法,可排除玻璃体积血、视网膜脱离和眼内肿瘤等疾患。在晶状体明显混浊,眼底镜检查不能辨明眼底情况时尤为重要(图7,8,9)。
 4.眼部特殊检查 对手术效果存在疑虑或有特殊要求,怀疑合并其他眼病的患者,要进行相关的检查。 (1)角膜内皮细胞检查:观察细胞密度(Cell density,CD)和六边型细胞(Hexagocyte)的比例。角膜内皮低于1000/mm2时,应慎重考虑白内障手术方式,以避免出现术后角膜失代偿而影响手术效果及术后恢复(图10,11)。
4.眼部特殊检查 对手术效果存在疑虑或有特殊要求,怀疑合并其他眼病的患者,要进行相关的检查。 (1)角膜内皮细胞检查:观察细胞密度(Cell density,CD)和六边型细胞(Hexagocyte)的比例。角膜内皮低于1000/mm2时,应慎重考虑白内障手术方式,以避免出现术后角膜失代偿而影响手术效果及术后恢复(图10,11)。 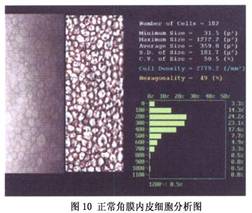
 临床主要应用于晶状体核过硬或不正常角膜内皮细胞人群如高龄老人(80岁以上)、二次内眼手术病人、合并角膜病变的患者以及有眼部外伤史的病人。 (2)视网膜视力检查:把特定的图像或视标投射到视网膜上,无论屈光间质是否混浊,直接检查视网膜的视力,以了解患者手术后可能达到的最佳视力,是术前评价黄斑功能的一种重要检查方法。常用的有2种方法:①激光视网膜视力仪:应用激光干涉原理,光穿过混浊屈光间质之间的透明裂隙,让病人辨认不同空间频率的平行线条的方向而得出视力。②潜在视力仪(Potential acuity meter,PAM):通过晶状体混浊的透明部位,投射0.1mm的点光源到视网膜,内含Snellen视力表视标让病人辨认而得出视力。这2种方法得到的视力大致相当于病人的术后视力,但在一些情况下与手术后患者恢复的视力有明显的差异:①混浊致密的白内障、玻璃体积血、散瞳不充分的患者,因光线穿透力有限,视网膜视力一般低于术后视力。当术前视力有0.1或以上时,90%的患者测出的视网膜视力大致等于手术后的视力(在两行视标以内);当术前视力低于0.1时,仅有60%的患者测出的视网膜视力与术后视力相符。②特殊眼底改变的患者,如高度近视者或黄斑水肿患者等,其视网膜视力可能高于术后视力。因为这些患者视网膜视力多在0.5以下,而远离黄斑中心凹的光感受器也能产生0.3~0.5的视力(图12)。临床主要应用于欲了解术后视力的病人以及怀疑眼底病变影响视力的病人。
临床主要应用于晶状体核过硬或不正常角膜内皮细胞人群如高龄老人(80岁以上)、二次内眼手术病人、合并角膜病变的患者以及有眼部外伤史的病人。 (2)视网膜视力检查:把特定的图像或视标投射到视网膜上,无论屈光间质是否混浊,直接检查视网膜的视力,以了解患者手术后可能达到的最佳视力,是术前评价黄斑功能的一种重要检查方法。常用的有2种方法:①激光视网膜视力仪:应用激光干涉原理,光穿过混浊屈光间质之间的透明裂隙,让病人辨认不同空间频率的平行线条的方向而得出视力。②潜在视力仪(Potential acuity meter,PAM):通过晶状体混浊的透明部位,投射0.1mm的点光源到视网膜,内含Snellen视力表视标让病人辨认而得出视力。这2种方法得到的视力大致相当于病人的术后视力,但在一些情况下与手术后患者恢复的视力有明显的差异:①混浊致密的白内障、玻璃体积血、散瞳不充分的患者,因光线穿透力有限,视网膜视力一般低于术后视力。当术前视力有0.1或以上时,90%的患者测出的视网膜视力大致等于手术后的视力(在两行视标以内);当术前视力低于0.1时,仅有60%的患者测出的视网膜视力与术后视力相符。②特殊眼底改变的患者,如高度近视者或黄斑水肿患者等,其视网膜视力可能高于术后视力。因为这些患者视网膜视力多在0.5以下,而远离黄斑中心凹的光感受器也能产生0.3~0.5的视力(图12)。临床主要应用于欲了解术后视力的病人以及怀疑眼底病变影响视力的病人。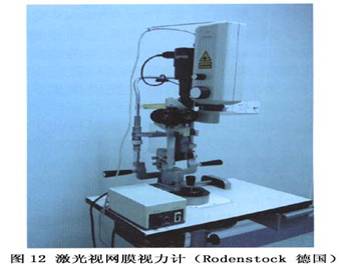 (3)视野检查:对于晶状体混浊较轻而具有一定视力的患者,进行视野检查可发现合并白内障的其他疾病。如中心暗点要警惕黄斑病变的存在,生理盲点的扩大及视野特征性的缺损要警惕青光眼及其他眼底病变的存在。由于白内障也会引起视野的改变,因此要联系裂隙灯观察到的晶状体混浊的部位而加以鉴别(图13)。
(3)视野检查:对于晶状体混浊较轻而具有一定视力的患者,进行视野检查可发现合并白内障的其他疾病。如中心暗点要警惕黄斑病变的存在,生理盲点的扩大及视野特征性的缺损要警惕青光眼及其他眼底病变的存在。由于白内障也会引起视野的改变,因此要联系裂隙灯观察到的晶状体混浊的部位而加以鉴别(图13)。  (4)视网膜电流图(ERG)检查:目前有闪光、图形和多焦3种ERG,可记录视网膜的视锥细胞功能、视杆细胞功能和混合功能。闪光ERG反映了整个视网膜的功能。图形ERG主要反映黄斑的功能。多焦ERG能同时记录中央30°视野内100多个视网膜位点上的ERG,有利于诊断和判断术后视网膜的功能状况。临床上常应用的是闪光ERG,如术前ERG正常或轻度降低,估计术后视力恢复较好,如果术前ERG明显降低或记录不到,估计术后的视力恢复不理想(图14,15)。
(4)视网膜电流图(ERG)检查:目前有闪光、图形和多焦3种ERG,可记录视网膜的视锥细胞功能、视杆细胞功能和混合功能。闪光ERG反映了整个视网膜的功能。图形ERG主要反映黄斑的功能。多焦ERG能同时记录中央30°视野内100多个视网膜位点上的ERG,有利于诊断和判断术后视网膜的功能状况。临床上常应用的是闪光ERG,如术前ERG正常或轻度降低,估计术后视力恢复较好,如果术前ERG明显降低或记录不到,估计术后的视力恢复不理想(图14,15)。
 临床主要应用于视网膜色素变性或全视网膜脱离者,表现为明视和暗视反应的降低甚至消失。视网膜血管性病变的患者主要表现为振荡电位降低。但是对非常致密白内障进行ERG检查时,由于光线较难到达视网膜,因此会出现假阳性结果。 (5)视觉诱发电位检查(VEP):VEP包括闪光VEP和图形VEP,用于记录从视网膜到视皮质的神经通路功能。当黄斑部和视神经出现病变时,可表现为振幅的降低和潜伏期的延长。当患者术前视力小于0.1时,一般采用闪光VEP检查。而患者视力较好时,可采用图形VEP检查。因此在晶状体明显混浊时,VEP检查对术后视功能的恢复程度具有较准确的预测性。 (6)光学相干断层扫描仪检查:应用近红外光进行眼前后段结构的断层扫描,是一种高分辨率横截面成像的影像学检查方法。它可在活体内直观显示视网膜各层的细微结构,特别是对于黄斑部疾病的诊断具有显著的临床价值(图16)。
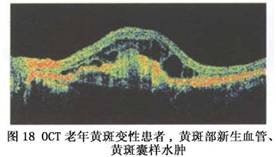
临床主要应用于视网膜色素变性或全视网膜脱离者,表现为明视和暗视反应的降低甚至消失。视网膜血管性病变的患者主要表现为振荡电位降低。但是对非常致密白内障进行ERG检查时,由于光线较难到达视网膜,因此会出现假阳性结果。 (5)视觉诱发电位检查(VEP):VEP包括闪光VEP和图形VEP,用于记录从视网膜到视皮质的神经通路功能。当黄斑部和视神经出现病变时,可表现为振幅的降低和潜伏期的延长。当患者术前视力小于0.1时,一般采用闪光VEP检查。而患者视力较好时,可采用图形VEP检查。因此在晶状体明显混浊时,VEP检查对术后视功能的恢复程度具有较准确的预测性。 (6)光学相干断层扫描仪检查:应用近红外光进行眼前后段结构的断层扫描,是一种高分辨率横截面成像的影像学检查方法。它可在活体内直观显示视网膜各层的细微结构,特别是对于黄斑部疾病的诊断具有显著的临床价值(图16)。 临床应用于怀疑黄斑裂孔(图17)、老年黄斑变性(图18)、视网膜前膜(图19)的病人。
临床应用于怀疑黄斑裂孔(图17)、老年黄斑变性(图18)、视网膜前膜(图19)的病人。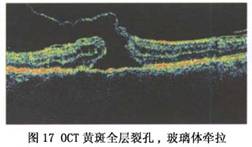
 (7)眼底检查及眼底血管造影检查:条件允许时可以考虑进行。 ①眼底检查:应用直接眼底镜或间接眼底镜的红光反射法,了解晶状体混浊程度。通过眼底镜检查,排除眼底病变尤其是当晶状体混浊与视力下降不符时。影响术后视力恢复的常见眼底改变有:A.糖尿病视网膜病变(图20);B.高度近视眼底病变(图21);C.老年性黄斑病变(图22);D.黄斑裂孔(图23);E.视网膜中央静脉阻塞(图24);F.缺血性视神经病变(图25);G.视网膜脱离(图26)。
(7)眼底检查及眼底血管造影检查:条件允许时可以考虑进行。 ①眼底检查:应用直接眼底镜或间接眼底镜的红光反射法,了解晶状体混浊程度。通过眼底镜检查,排除眼底病变尤其是当晶状体混浊与视力下降不符时。影响术后视力恢复的常见眼底改变有:A.糖尿病视网膜病变(图20);B.高度近视眼底病变(图21);C.老年性黄斑病变(图22);D.黄斑裂孔(图23);E.视网膜中央静脉阻塞(图24);F.缺血性视神经病变(图25);G.视网膜脱离(图26)。

 浙公网安备
33010902000463号
浙公网安备
33010902000463号



